Was ist LAL-D?
Lysosomale saure Lipase-Defizienz (LAL-D) ist eine seltene erbliche Stoffwechselerkrankung. Bei LAL-D besteht ein Mangel des Enzyms lysosomale saure Lipase (LAL). Dadurch werden Fette und Cholesterinester übermäßig in verschiedenen Geweben angehäuft, was wiederum zu Organschäden führt.
Lysosom = Zellorganellen, die Enzyme enthalten, mit denen Fremdstoffe oder körpereigene Stoffe abgebaut werden. Man spricht deshalb auch vom „Magen der Zelle“.
Lysosomale saure Lipase = Enzym, das nur im Lysosom Fette spaltet
Defizienz = Mangel bzw. Mangelfunktion
Häufigkeit der Erkrankung
Genaue Zahlen sind nicht bekannt. Abhängig von der ethnischen Zugehörigkeit und der geografischen Herkunft, liegt die Prävalenz für LAL-D schätzungsweise zwischen 1:40.000 und 1:300.000.ref_synoracki_2018 Sie zählt damit zu den seltenen Erkrankungen (orphan diseases).
Erkrankungsalter
LAL-D kann in allen Altersgruppen auftreten. Liegt eine verminderte Aktivität von LAL vor, kann die Erkrankung im Kindes- und Erwachsenenalter zu Symptomen führen. Bei den meisten Patienten zeigen sich erste Anzeichen der Erkrankung schon vor dem 12. Lebensjahr.
Bei einer drastischen Reduktion oder Fehlen des Enzyms LAL tritt die Erkrankung bereits im Säuglingsalter zutage und wird historisch auch als Morbus Wolman bezeichnet. Diese frühe Ausprägung ist besonders schwerwiegend.
Geschlecht
LAL-D tritt geschlechtsunspezifisch auf.
Was passiert bei LAL-D?
Die Verstoffwechslung von Fetten und Cholesterinverbindungen findet in den Lysosomen unserer Körperzellen statt mit Hilfe des Enzyms lysosomale saure Lipase (LAL). Die gespalteten Verbindungen kann der Körper weiter verwerten.
Bei Patient:innen mit LAL-D ist dieser Stoffwechselvorgang durch einen Enzymmangel gestört. Die Ursachen dafür sind verschiedene Mutationen im LIPA-Gen, so dass kein oder zu wenig LAL zur Verfügung steht. Die Lipide und Cholesterinverbindungen können daher nicht weiter verstoffwechselt werden. Stattdessen werden sie in den Zellen eingelagert, wodurch die Zellen verfetten.
Außerdem ist das Cholesteringleichgewicht innerhalb der Zellen gestört. Aufgrund der beeinträchtigten Lipidspaltung fehlen der Zelle die Abbauprodukte aus dem Lysosom wie z.B. das freie Cholesterin. Die Leberzellen versuchen, diesen Mangel durch eine vermehrte eigene Herstellung von Cholesterin zu kompensieren. Dies führt zu erhöhten Cholesterinwerten (LDLCholesterin) im Blut. Die Folge ist ein erhöhtes Risiko für eine Arterienverkalkung und eine koronare Herzkrankheit. Dadurch steigt das Risiko für die Patienten, einen Herzinfarkt oder einen Schlaganfall zu erleiden.
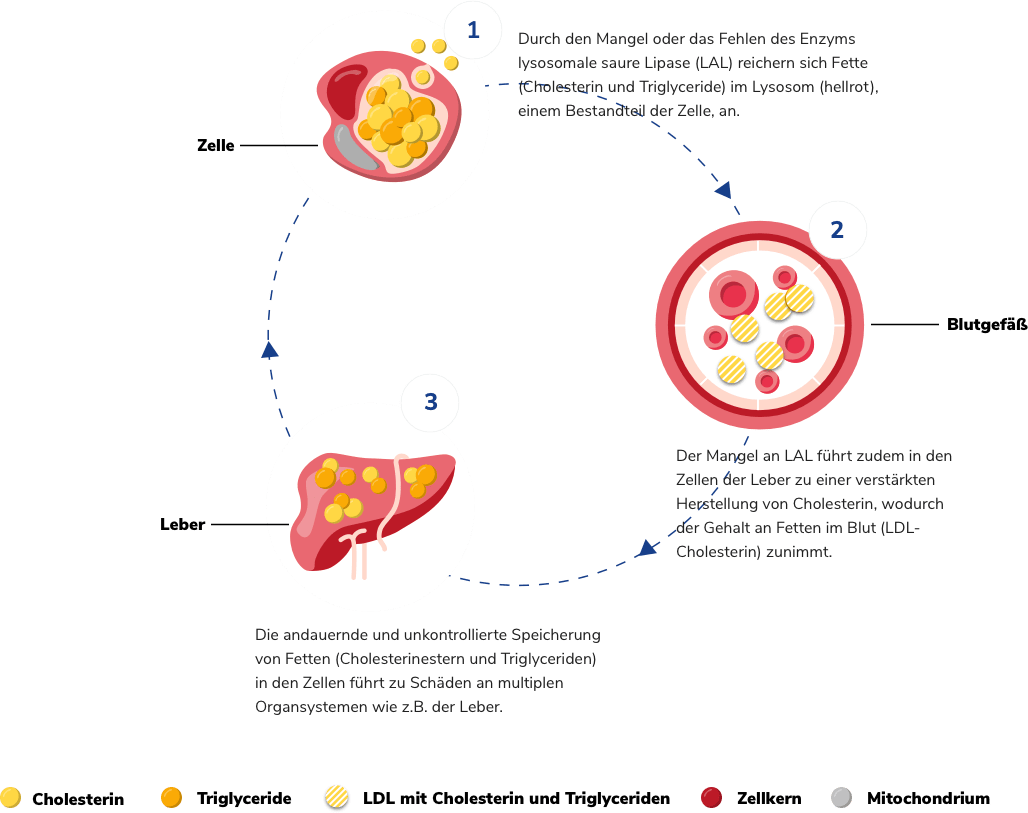
Durch die vermehrte Einlagerung von Cholesterin und Triglyceriden in den Leberzellen werden diese in ihrer Funktion zunehmend geschädigt. Auch in anderen Organen wie der Milz oder dem Magen-Darm-Trakt kommt es zu Schäden und Beeinträchtigungen durch LAL-D.
Das Schaubild verdeutlicht die Vorgänge im Körper:
Klinisches Bild

Dyslipidämie – veränderter Gehalt an Cholesterin und Fetten im Blut
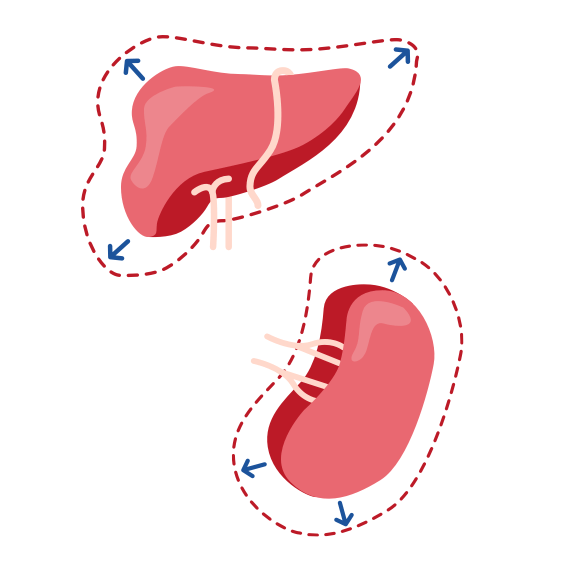
Vergrößerte Leber und Milz
Das klinische Bild der LAL-D ist leider unspezifisch. Die klinischen Befunde können jedoch einen wichtigen Hinweis auf das Vorliegen dieser seltenen Erkrankung liefern.
Der gestörte Fett- und Cholesterinstoffwechsel bei LAL-D wirkt sich auf die Blutwerte aus. Es lässt sich eine Dyslipidämie nachweisen, d.h. ein veränderter Gehalt an Cholesterin und eventuell Fetten im Blut. Der Spiegel des „guten“ HDL-Cholesterins ist erniedrigt, während das LDL-Cholesterin erhöht ist. Auch in den Organen zeigen sich die Folgen der Stoffwechselerkrankung und lassen sich messen. Die andauernde und unkontrollierte Speicherung von Cholesterin und Fetten in den Zellen führt in der Regel zu einer Vergrößerung und Schädigung von Leber und Milz.
Symptome
LAL-D gefährdet verschiedene lebenswichtige Organe, unter anderem die Leber, das Herz, die Milz und den Magen-Darm-Trakt. Bei den meisten Patient:innen (87%)ref_bernstein_2013 sind mehrere Organe von der Erkrankung betroffen. Die Leber ist am häufigsten involviert. Die Symptome dieser seltenen Stoffwechselerkrankung sind oft unspezifisch und können von Patient:in zu Patient:in unterschiedlich sein.
Symptome, die die Leber betreffen, sind z.B.

• Vergrößerung der Leber
• Veränderung der Leberstruktur wie z. B. Leberfibrose (narbige Veränderung) bis zur Zirrhose (narbige Schrumpfung der Leber) und Leberversagen
• Gelbsucht aufgrund einer Schädigung der Leberzellen
Symptome, die das Herz-Kreislauf-System betreffen, sind z.B.

• Erkrankung der Herzkranzgefäße
• Bluthochdruck
• Schlaganfall
Symptome, die die Milz betreffen, sind z.B.

• Mangel an Blutplättchen und roten Blutkörperchen aufgrund der Funktionsstörung der Milz
Symptome, die den Magen-Darm-Trakt betreffen, sind z.B.

• Erbrechen
• Durchfall
• Gedeihstörungen bei Säuglingen und Kindern
• Wachstumsdefizite
Bei Säuglingen mit schwerem Mangel oder Fehlen des Enzyms LAL, äußert sich die LAL-D typischerweise durch Gedeihstörung mit anhaltendem Erbrechen in Kombination mit schweren Durchfällen. Leber und Milz sind vergrößert und in ihrer Funktion beeinträchtigt. Es zeigt sich in vielen Fällen eine Verkalkung der Nebennieren. Der schnell fortschreitende Verlauf der Erkrankung kann lebensbedrohlich sein.
Diagnose der LAL-D
Bei seltenen Erkrankungen wie LAL-D kann es mehrere Jahre dauern, bis die korrekte Diagnose gestellt wird. Das liegt daran, dass die Symptome der Erkrankung nicht spezifisch sind, d. h. sie gleichen den Symptomen anderer Erkrankungen. In Blutuntersuchungen zeigen sich typischerweise erhöhte Leberenzyme kombiniert mit hohen LDL-Cholesterin- und erniedrigten HDL-Cholesterinspiegeln sowie hohen Triglyceridwerten (Dyslipidämie). Sowohl häufigere Lebererkrankungen als auch andere seltene Stoffwechselerkrankungen wie z. B. Morbus Wilson oder Morbus Gaucher sind während der Diagnostik auszuschließen.
LAL-D kann durch einen einfachen Bluttest, der die Enzymaktivität der lysosomalen sauren Lipase misst, diagnostiziert werden. Zusätzlich kann die Diagnose durch den Nachweis einer Mutation im LIPA-Gen gesichert werden.
Behandlung der LAL-D
In der Therapie der lysosomalen sauren Lipase-Defizienz stehen derzeit unterstützende Behandlungen zur Verfügung wie
- diätetische Maßnahmen wie z. B. eine fettreduzierte Ernährung
- bestimmte lipidsenkende Medikamente wie z.B. Statin-Therapien (Arzneimittel, das den Gehalt an Fetten im Blut senkt)
- Lebertransplantation und
- Transplantation von Blutstammzellen.
Zur Behandlung von LAL-D steht außerdem eine Enzymersatztherapie zur Verfügung, die die Ursachen der Erkrankung bekämpft. Hierbei wird der/m Patientin/en in regelmäßigen Abständen – altersabhängig entweder wöchentlich oder alle zwei Wochen – per Infusion ein Medikament verabreicht, das die fehlende Enzymaktivität der lysosomalen sauren Lipase ersetzt. Die Therapie wird auf die individuelle Symptomatik der Patient:innen abgestimmt.
Wie stark das tägliche Leben eingeschränkt ist, hängt von der jeweiligen Ausprägung der LAL-D ab. Wichtig ist, konsequent auf eine angemessene Ernährung zu achten. Eine Ernährungsberatung hilft Betroffenen, die Zufuhr von Cholesterin und gesättigten Fettsäuren zu reduzieren.
Glossar
| Cholesterin | Lipidähnliche Substanz und wird im Körper in Form von Partikeln transportiert, z. B. LDL. |
| HDL-Cholesterin | Abkürzung für High Density Lipoprotein, wird für den Cholesterintransport zur Leber benötigt |
| LDL-Cholesterin | Abkürzung für Low Density Lipoprotein, transportiert Cholesterin von der Leber zu den Körperzellen. Hohe LDL-C-Spiegel fördern Arteriosklerose. |
| Cholesterinester |
Ein Stoffwechselzwischenprodukt: Chemische Verbindung zwischen Cholesterin und einer Fettsäure |
| Defizienz | Mangel bzw. Mangelfunktion |
| Dyslipidämie |
Eine Veränderung der Zusammensetzung der Blutfette. |
| Enzym | Ein biochemischer Katalysator für spezifische Vorgänge im Stoffwechsel. |
| Lysosomen | Zellorganellen, die Enzyme enthalten, mit denen Fremdstoffe oder körpereigene Stoffe abgebaut werden – „Magen der Zelle“ |
| Lysosomale saure Lipase | Ein Enzym im Lysosom, das Fette und Cholesterinverbindungen spaltet |
| Morbus |
Die lateinische Bezeichnung für Krankheit. Häufig wird die Bezeichnung Morbus in Zusammenhang mit dem Erstbeschreiber der Erkrankung verwendet, z.B. Morbus Wolman |
| Mutation |
Die Veränderung des Erbguts in einem Organismus |
| Prävalenz | Häufigkeit der Erkrankungen in einer Bevölkerung zu einem bestimmten Zeitpunkt |
| Stammzellen |
Noch nicht spezialisierte Körperzellen. Je nach Art der Stammzelle und ihrer Beeinflussung haben sie das Potenzial, sich in alle Zelltypen (embryonale Stammzellen) oder in bestimmte festgelegte Gewebetypen (adulte Stammzellen wie z.B. Blutstammzellen) zu entwickeln |
| Statine | Medikamente, die die Konzentration von Cholesterin im Blut senken. |
| Triglyceride | Sind Verbindungen in Fetten oder fetten Ölen. Sie dienen dem Körper als Energiereserve und werden im Körper zum Transport in eiweißhaltige Partikel verpackt (z. B. LDL) |
Weiterführende Inhalte zu LAL-D
Referenzen
- Synoracki, S., Kathemann, S., Schmid, K.W. et al. 2018. Mangel an lysosomaler saurer Lipase (LAL-D). Pathologe 39, 249–254. https://doi.org/10.1007/s00292-017-0400-z.
- Bernstein, Donna L., Helena Hülkova, Martin G. Bialer, und Robert J. Desnick. 2013. „Cholesteryl Ester Storage Disease: Review of the Findings in 135 Reported Patients with an Underdiagnosed Disease“. Journal of Hepatology 58 (6): 1230–43. https://doi.org/10.1016/j.jhep.2013.02.014.
weitere referenzen
Burton, Barbara K., Manisha Balwani, François Feillet, Ivo Barić, T. Andrew Burrow, Carmen Camarena Grande, Mahmut Coker, u. a. 2015. „A Phase 3 Trial of Sebelipase Alfa in Lysosomal Acid Lipase Deficiency“. New England Journal of Medicine 373 (11): 1010–20. https://doi.org/10.1056/NEJMoa1501365.
Burton, Barbara K., Patrick B. Deegan, Gregory M. Enns, Ornella Guardamagna, Simon Horslen, Gerard K. Hovingh, Steve J. Lobritto, u. a. 2015. „Clinical Features of Lysosomal Acid Lipase Deficiency“. Journal of Pediatric Gastroenterology and Nutrition 61 (6): 619–25. https://doi.org/10.1097/MPG.0000000000000935.
Burton, Barbara K., Nancy Silliman, und Sachin Marulkar. 2017. „Progression of Liver Disease in Children and Adults with Lysosomal Acid Lipase Deficiency“. Current Medical Research and Opinion 33 (7): 1211–14. https://doi.org/10.1080/03007995.2017.1309371.
Jones, Simon A., Sandra Rojas-Caro, Anthony G. Quinn, Mark Friedman, Sachin Marulkar, Fatih Ezgu, Osama Zaki, u. a. 2017. „Survival in Infants Treated with Sebelipase Alfa for Lysosomal Acid Lipase Deficiency: An Open-Label, Multicenter, Dose-Escalation Study“. Orphanet Journal of Rare Diseases 12 (1): 25. https://doi.org/10.1186/s13023-017-0587-3.
Jones, Simon A., Vassili Valayannopoulos, Eugene Schneider, Stephen Eckert, Maryam Banikazemi, Martin Bialer, Stephen Cederbaum, u. a. 2016. „Rapid Progression and Mortality of Lysosomal Acid Lipase Deficiency Presenting in Infants“. Genetics in Medicine: Official Journal of the American College of Medical Genetics 18 (5): 452–58. https://doi.org/10.1038/gim.2015.108.
Reiner, Željko, Ornella Guardamagna, Devaki Nair, Handrean Soran, Kees Hovingh, Stefano Bertolini, Simon Jones, u. a. 2014. „Lysosomal Acid Lipase Deficiency--an under-Recognized Cause of Dyslipidaemia and Liver Dysfunction“. Atherosclerosis 235 (1): 21–30. https://doi.org/10.1016/j.atherosclerosis.2014.04.003.
Vijay, Suresh, Anais Brassier, Arunabha Ghosh, Simona Fecarotta, Florian Abel, Sachin Marulkar, und Simon A. Jones. 2021. „Long-Term Survival with Sebelipase Alfa Enzyme Replacement Therapy in Infants with Rapidly Progressive Lysosomal Acid Lipase Deficiency: Final Results from 2 Open-Label Studies“. Orphanet Journal of Rare Diseases 16 (1): 13. https://doi.org/10.1186/s13023-020-01577-4.